 |
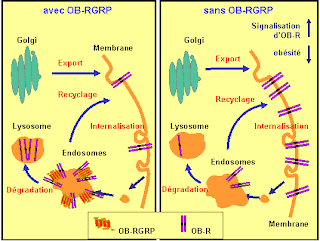
| [En marge de la présente communication]: (...) De nouvelles données indiquent que la protéine OB-RGP serait une nouvelle cible pour le traitement de l'obésité (...) L'obésité est une préoccupation majeure de santé publique dans nos sociétés modernes. Elle est particulièrement liée au développement du diabète de type 2 (...). Source: http://cochin.inserm.fr/l_actualite/evenements-des-annees-precedentes/ob-rgrp-regulateur-negatif-du-recepteur-de-la |
L'activation du récepteur aux acides gras 1 (FFAR1, désigné aussi sous l'appellation récepteur 40 couplé aux protéines G) par les acides gras a montré une sécrétion d'insuline par les cellules beta glucose-dépendante dans les modèles précliniques. Notre but était d'étudier si une activation pharmacologique sélective de ce récepteur par le TAK-875 chez les patients atteints de diabète de type 2 pouvait améliorer le contrôle de la glycémie sans risque d'hypoglycémie.
Nous avons effectué une étude de phase 2, randomisée, en double-aveugle, contrôlée par placebo et par agent de comparaison, chez des patients en ambulatoire atteints de diabète de type 2 ne répondant pas à un régime alimentaire ou à la metformine. Les patients ont été distribués de manière aléatoire dans des groupes pour recevoir le placebo, le TAK-875 (6,25; 25; 50; 100 ou 200 mg) ou le glimepiride, une fois par jour pendant 12 semaines. Ni les patients ni les investigateurs n'avaient accès au tableau de distribution des traitements. Le paramètre principal mesuré suite aux traitements était l'évolution des taux d'hémoglobine A1c (HbA1c) par rapport à la ligne de base. L'analyse a inclus tous les patients recrutés et assignés à un groupe, et qui ont reçu au moins une dose du médicament à l'étude. (...).
426 patients ont été distribués de manière aléatoire pour recevoir le TAK-875 (n=303), le placebo (n=61), et le glimepiride (n=62). A t = semaine 12, une diminution significative de HbA1c par rapport à la ligne de base a été mesurée, chez tous les patients des groupes TAK-875 (s'échelonnant de -1,12% [Erreur Standard SE = 0,113] avec 50 mg à -0,65% [0,114] avec 6,25 mg) et du groupe glimepiride (-1,05% [ES = 0,111]) versus placebo (-0,13% [SE = 0,115]); valeurs de p s'échelonnant entre p = 0,001 et p < 0,0001) (méthode des moindres carrés).
Les évènements hypoglycémiques dûs au traitement étaients similaires dans les groupes TAK-875 et placebo (2% [n = 7; tous groupes TAK-875] versus 3% [n = 2]); des taux plus élevés étant observés pour le groupe glimepiride (19% [n = 12]; valeurs de p s'échelonnant entre de p = 0,010 à p = 0,002 versus tous groupes TAK-875). L'incidence des évènements indésirables dûs aux traitements était similaire dans tous les groupes TAK-875 (49%, n = 147, tous groupes TAK-875) et placebo (48%, n = 29) et était plus bas dans le groupe glimepiride (61%, n = 38).
Le TAK-875 a amélioré de manière significative le contrôle de la glycémie, avec un risque d'hypoglycémie minimum. Les résultats montrent que l'activation de FFAR1 est une cible thérapeutique viable pour le traitement du diabète de type 2. Prof Charles F Burant MD, in The Lancet, Early Online Publication 27 February 2012
Source: http://www.thelancet.com/ / Traduction et adaptation: NZ
Aucun commentaire:
Enregistrer un commentaire