 |
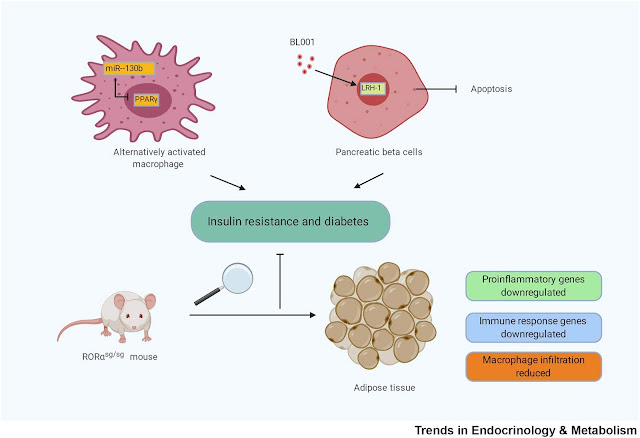
Modèle Schématique
du Mécanisme de Régulation de l’Immunité dans le Développement de la Résistance
à l’Insuline et le Diabète*.
Le PPARƳ des cellules myéloïdes bloque l’activation
des macrophages alternatifs, contribuant aux altérations métaboliques
fonctionnelles comprenant notamment l’obésité provoquée par un régime
alimentaire, la résistance à l’insuline, et l’intolérance au glucose chez les
modèles de souris. De plus, lorsqu’exposée à un régime alimentaire riche en
lipides, la régulation positive de miR-130b dans les macrophages soumet à
régulation à la fois la polarisation M1/M2, l’inflammation du tissu adipeux, et
la tolérance au glucose par le truchement du récepteur PPARƳ. L’activation
de LRH-1 par BL001 retarde l’inflammation pancréatique et l’apparition de l’hyperglycémie
chez les modèles de souris diabétiques de type 1 tout en réduisant la mort
cellulaire par apoptose des cellules ß-pancréatiques et augmentant la
sécrétion d’insuline chez les modèles de diabète de type 2. Les souris RORα-déficientes
soumises à un régime alimentaire riche en lipides présentent une diminution des
contenus en triglycérides dans le tissu adipeux et dans le foie en comparaison
de leurs congénères de types sauvage. Une déficience en RORα réduit l’infiltration
en macrophages et l’expression des gènes de l’inflammation dans le tissu
adipeux blanc, tout en protégeant les souris d’une résistance à l’insuline et
augmentant la dépense énergétique et le métabolisme des animaux. (…).
Abréviations : miR, microARN ; PPARƳ, récepteur activé par les
proliférateurs des peroxysomes Ƴ ; RORα, récepteur orphelin lié à l’acide
rétinoïque α.
|
Les membres de la superfamille des récepteurs
nucléaires servent de régulateurs majeurs dans la signalisation, par la
régulation soit positive, soit négative de l’expression génique. Des preuves
toujours plus nombreuses suggèrent que les récepteurs nucléaires sont fortement
impliqués dans les réponses immunitaires, avec des rôles spécifiques dans différents
compartiments des cellules immunocompétentes, contribuant à la fois aux fonctions physiologiques normales et au développement des maladies. Les propriétés thérapeutiques des
récepteurs nucléaires en ont fait des cibles thérapeutiques modulables idéales.
Ici, nous revisitons la biologie des récepteurs nucléaires, résumons les
avancées récentes dans notre compréhension des fonction immunologiques des
récepteurs nucléaires, et décrivons les rôles type cellulaire-spécifiques et
des récepteurs nucléaires spécifiques dans la pathogénèse des maladies, et
explorons leur potentiel comme cible thérapeutique nouvelle. Ces altérations
récepteur-nucléaire-dépendantes du système immunitaire sont accessibles aux
manipulations pharmacologiques et suggèrent de nouvelles stratégies
thérapeutiques. Linjie Zhao, et al, dans Trends in Endocrinology and
Metabolism, publication en ligne en avant-première, 6 novembre 2019
Source iconographique, légendaire et rédactionnelle :
Science Direct / Traduction et
adaptation : NZ
*Il est possible d'augmenter la définition de l'image ci-dessus en cliquant dessus (note de l'éditeur de ce post).




