Un tissu
adipeux sain et essentiel à un bon fonctionnement du métabolisme. Cette donnée
est provient de ce que l’on connaît de l’épidémie d’obésité, avec sa myriade de comorbidités associées à un excès de tissu adipeux incluant
diabète de type 2, maladie cardiovasculaire et cancer.
La lipodystrophie est
une cause de résistance à l’insuline, amplifiant l’importance d’une proportion
appropriée de tissu adipeux dans l’organisme. Dans les cellules, la cible fonctionnelle
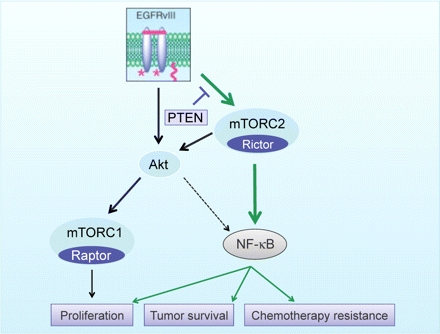
des complexes mTOR 1 et 2 (mTORC1 et mTORC2
respectivement) lient les signalisations nutritionnelle et hormonale avec le
métabolisme, et de récentes études apportent un nouvel éclairage sur les rôles
des adipocytes in vivo. Dans cette
revue de littérature, nous discutons des connaissances nouvelles concernant le
mode de convergence des nouveaux mécanismes permettant de maintenir un tissu
adipeux sain, et discutons des mystères de la signalisation mTOR restant à
décrypter, pour ce qui est notamment du complexe mTORC2, le moins connu. Peter
L. Lee, et al, dans Trends in Endocrinology and Metabolism, publication en
ligne en avant-première, 22 février 2017