|
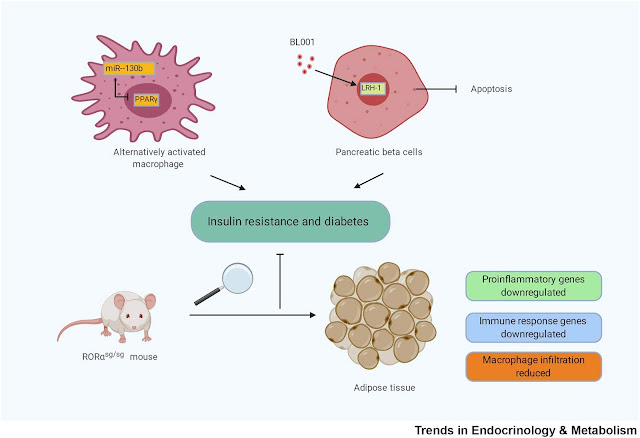
| Le brunissement du tissu adipeux brun provoque une augmentation de la thermogenèse, laquelle diminue l'obésité. Un mécanisme concomitant induit la stabilisation des ARNm des gènes thermogéniques. |
La graisse beige joue un rôle clé dans la régulation de l'homéostasie énergétique systémique ; cependant, les mécanismes détaillés et la stratégie sûre pour son activation restent insaisissables. Dans cette étude, nous avons découvert que la thérapie par hyperthermie locale (LHT) ciblant la graisse beige favorisait son activation chez l'homme et la souris. LHT obtenu à l'aide d'une thérapie photothermique à base d'hydrogel activé la graisse beige, prévenant et traitant l'obésité chez la souris sans effets indésirables. HSF1 est nécessaire pour les effets puisque la carence en HSF1 a émoussé les avantages métaboliques de la LHT. HSF1 régule la transcription de Hnrnpa2b1 (A2b1), conduisant à une stabilité accrue de l'ARNm des gènes métaboliques clés. Il est important de noter que l'analyse des études d'association humaine suivie d'une analyse fonctionnelle a révélé que le variant de gain de fonction HSF1 p.P365T est associé à une amélioration des performances métaboliques chez l'homme et à une transcription A2b1 accrue chez la souris et les cellules. Dans l'ensemble, nous démontrons que LHT offre une stratégie prometteuse contre l'obésité en induisant l'activation de la graisse beige via l'axe transcriptionnel HSF1-A2B1. Yu Li, et al, dans Cell, publication en ligne en avant-première, 4 mars 2022
Source iconographique, légendaire et rédactionnelle : Science Direct / Préparation post : NZ