 |
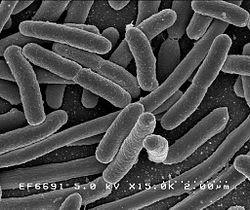
| Bactérie Escherichia coli pathogène Source iconographique: https://en.wikipedia.org/wiki/Pathogenic_Escherichia_coli |
ExPEC4V (JNJ-63871860) est un vaccin bioconjugué,
contenant les sérotypes O O1A, O2, O6A, O25B, développés pour la prévention contre
les infections extra-intestinales à E.coli (ExPEC) invasives pathogènes. Notre
but était d’évaluer l’innocuité, la réactogénécité et l’immunogénécité de
ExPEC4V chez des adultes sains.
Dans cet étude de phase 2 randomisée, en
double-aveugle, nous avons recruté des adultes sains (≥18 ans présentant un
indice de masse corporelle de 35 kg/m2 au plus) entre le 16 novembre
2015 et le 8 août 2017, et les avons assignés par tirage au sort pour recevoir
une dose unique de ExPEC4V (antigènes O1A :O2 :O6A :O25B à
raison de 4 :4 :4 :4 μg
[groupe 1] ; 4 :4 :4 :8 μg [groupe 2],
8 :8 :8 :8 μg [groupe 3], 8 :8 :8 :16 μg
[groupe 4], ou 16 :16 :16 :16 μg
[groupe 5] ou le placebo. L’objectif principal était l’évaluation de
l’innocuité, de la tolérance et de l’immunogénécité de ExPEC4V et la
détermination de son immunogénécité dose-dépendante par ELISA 15 jours après la
vaccination par chez les sujets qui avaient reçu au moins une dose de vaccin. Les
mesures du titre en anticorps et de l’innocuité ont été utilisées pour la
sélection des deux doses d’ExPEC4V pour l’évaluation jusqu’au jour 360. (…).
Sur les 848 participants recrutés, 843 (99%) ont
reçu le vaccin ExPEC4V (757) ou le placebo (86) ; ils ont été inclus dans
l’analyse d’innocuité. Sur les 757 participants vaccinés avec ExPEC4V, 222 (29%)
ont présenté des évènements indésirables surveillés locaux et 325 (43%) ont
présenté des évènements indésirables systémiques surveillés, en comparaison des
11 (13%) et 30 (35%) participants sur 86 du groupe de contrôle. Les symptômes
étaient d’intensité légère à modérée. L’ événement indésirable local surveillé
les plus communément rapporté était douleur et sensibilité (205 [27,1%]
participants sur les 757 des groupes ExPEC4V mutualisés) et l’événement
indésirable systémique surveillé le plus communément rapporté était fatigue
(208 [27,1%] participants sur 757). 13 (2%) participants seulement sur 843 ont
présenté un évènement de grade 3.
Au jour 15, 80% des participants, au moins, ont
obtenu un doublement ou plus de leur concentration en Immunoglobulines
sérotype-spécifiques (sauf O25B à la dose la plus faible, 103 [72%] sur 144).
Au jour 360, 66% (Intervalle de Confiance [IC] 95% 56.47-74.33) des
participants du groupe 2 et 71% (62.13-78.95) des participants du groupe 4
sélectionnés pour un suivi à long terme ont maintenu un doublement ou plus de
la concentration en anticorps sérotype-spécifiques en comparaison avec la ligne
de base.
EXPEC4V semble être bien toléré et a déclenché de
fortes réponses des anticorps, quels que soient les sérotypes, les doses, et
les groupes d’âge des participants. Pour les deux doses (4 :4 :4 :8
et 8 :8 :8 :16) évaluées, la réponse a persisté pendant une
année. Robert W Frenck, Jr, MD, et al, dans The Lancet Infectious Diseases,
publication en ligne en avant-première, 9 mai 2019
Financement : Janssen Pharmaceuticals
Source : The Lancet Online / Traduction et
adpatation : NZ
Aucun commentaire:
Enregistrer un commentaire