 |
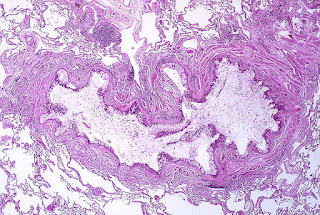
| Obstruction de la lumière d'une bronchiole par exsudation de mucus, métaplasie des cellules caliciformes, épaississement de la membrane basale et inflammation sévère des bronchioles Source: https://commons.wikimedia.org/wiki/File:Asthma_.jpg |
Il n’y a, à ce jour, aucune étude relative à l’efficacité
de la trithérapie administrée par inhalateur unique dans le traitement de l’asthme.
Ici, nous rendons compte de deux études comparant la combinaison de béclométasone
dipropionate (BDP ; corticostéroïde inhalé), formoterol fumarate (FF ;
agoniste ß2
à action prolongée), et glycopyrronium (G ; antagoniste muscarinique à
action prolongée) avec la combinaison de BDP avec FF.
Deux études de phase 3 à groupes parallèles, en double-aveugle,
randomisés, contrôlés par médicament actif (…), TRIMARAN et TRIGGER, ont
recruté des patients provenant de 171 sites situés dans 16 pays (TRIMARAN), et
de 221 sites situés dans 17 pays (TRIGGER). (…). Les patients éligibles étaient
adultes (âgés de 18 ans – à 75 ans) atteints d’asthme non contrôlé, avec historique
d’une exacerbation ou plusieurs exacerbations au cours de l’année précédente,
précédemment traitées à l’aide d’un corticostéroïde par inhalation (TRIMARAN :
dose moyenne ; TRIGGER : dose élevée) additionné d’un agoniste ß2
à action prolongée. Les patients recrutés avaient initialement reçu un
traitement BDP/FF (TRIMARAN : 100 μg
BDP et 6
μg FF ; TRIGGER : 200 μg BDP et 6 μg FF) pendant 2 semaines, puis
répartis au hasard dans les groupes de traitement à l’aide d’une technologie de
réponse interactive avec randomisation à disposition équilibrée des blocs selon
un schéma de stratification par pays. Ni les patients, ni les investigateurs,
ni le personnel du site, ni les représentants du sponsor de l’étude n’avaient
accès au tableau de randomisation.
Dans l’essai TRIMARAN, les patients étaient
répartis de manière aléatoire (1:1) pour recevoir BDF/FF/G (100 μg
BDP 6
μg FF, et 10 μg G) ou BDP/FF (100 μg BDP et 6 μg G), en deux inhalations deux
fois par jour pendant 52 semaines.
Dans l’essai TRIGGER, les patients étaient répartis
de manière aléatoire (2:2:1) pour recevoir BDP/FF/G (200 μg BDP, 6 μg et 10 μg
G) ou BDP/FF (200 μg BDP et 6 μg FF), les 2 combinaisons en deux inhalations
deux fois par jour plus 2.5 μg de tiotropium en deux inhalations
une fois par jour. Les principaux objectifs associés dans les deux essais (BDP/FF/G
versus BDP/FF) étaient le volume
expiratoire maximum en 1 seconde (VEMS) mesuré avant prise de médicament à la
semaine 26 et le taux d’exacerbation(s) modérée(s) et sévère(s) sur 52
semaines. L’innocuité était mesurée chez tous les patients qui avaient reçu au
moins une dose de médicament à l’étude. (…).
Du 17 février 2016 au 17 mai 2018, 1155
patients de l’essai TRIMARAN ont reçu BDP/FF/G (n=579) et BDP/FF (n=576).
Du 6 avril 2016 au 28 mai 2018, 1437 de l’essai TRIGGER ont reçu BDP/FF/G
(n=573), BDP/FF (n=576), ou BDP/FF plus tiotropium (n=288).
En comparaison avec
le groupe BDP/FF, la VEMS mesurée avant prise de médicament à la semaine 26 s’est
améliorée dans le groupe BDP/FF/G de 57 mL (Intervalle de Confiance [IC] 15-99 ;
p=0.0080) dans l’étude TRIMARAN et
de 73 mL (26-120 ; p=0.0025)
dans l’étude TRIGGER, avec des réductions de 15% des taux d’exacerbations
modérées et sévères (ratio des taux 0.85, IC 95% 0.73-0.99 ; p=0.033) dans
l’essai TRIMARAN et de 12% (0.88, 0.75-1.03 ; p=0.11) dans l’essai TRIGGER.
Quatre patients ont présenté des
évènements indésirables graves liés au traitement, un dans le groupe BDP/FF/G
de l’essai TRIMARAN et trois – un dans le groupe BDP/FF/G et deux dans le
groupe BDP/FF - de l’essai TRIGGER. Trois patients du groupe BDP/FF/G de l'essai TRIMARAN et deux patients de l'essai TRIGGER - un du groupe BDF/FF/G et un du groupe BDP/FF - ont présenté des évènements indésirables
menant à un décès. Aucun des décès n’a été imputé au traitement.
Dans l’asthme non contrôlé, l’ajout d’un
antagoniste muscarinique à action prolongée aux corticostéroïdes inhalés
plus un agoniste ß2 à action prolongée améliore la fonction
pulmonaire tout en diminuant les exacerbations. Prof Johann Christian Virchow,
MD, et al, dans The Lancet, publication en ligne en avant-première, 30
septembre 2019
Financement :
Chiesi Farmaceutici
Source :
The Lancet Online / Traduction et adaptation :
NZ
Aucun commentaire:
Enregistrer un commentaire